Què passa des que es descobreix una substància amb possibles efectes terapèutics fins que el medicament arriba a les vostres mans?
El procés de desenvolupament d’un fàrmac és llarg, complex i costós. Per tal que l'administració competent n’aprovi la comercialització i l’ús, cal que l’empresa farmacèutica demostri, mitjançant els resultats de diversos estudis d’investigació, que el nou medicament és de qualitat, eficaç i segur per a qui vagi destinat.
La creació d'un nou fàrmac comença en el moment en què una molècula química pot tenir aplicacions interessants en medicina. A partir d’aquí es diferencien dues grans fases:
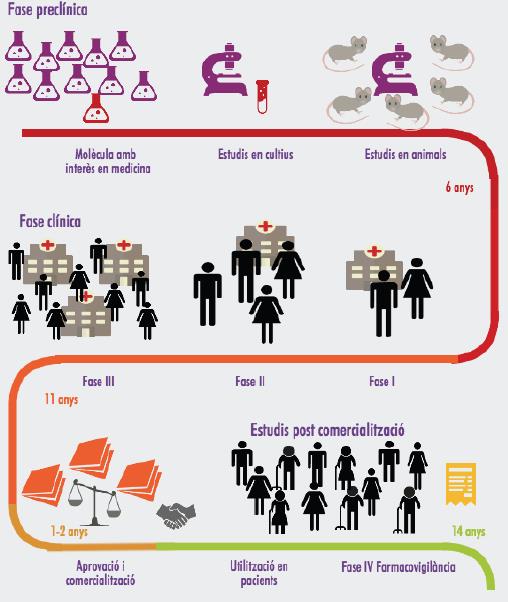
FASE PRECLÍNICA: no es realitzen proves en humans, sinó que es porten a terme estudis en cultius (in vitro) i en animals de laboratori (in vivo). L’objectiu és conèixer com funciona la molècula estudiada, el seu efecte en un organisme viu a diferents dosis i si és tòxica, abans de provar-la en humans.
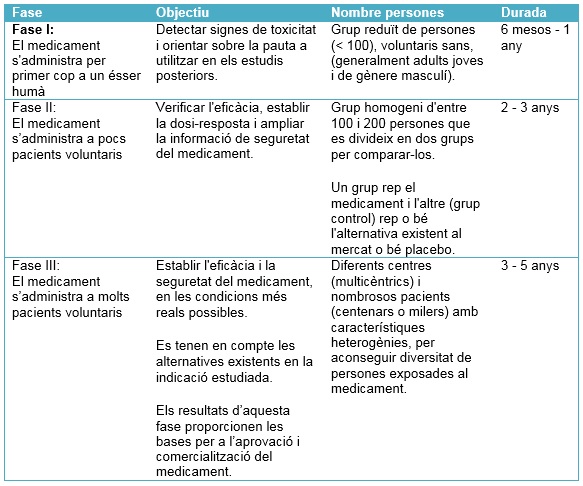
FASE CLÍNICA: es porten a terme assajos clínics en humans. Serveix per provar l'eficàcia terapèutica de la molècula i defineix la formulació que donarà lloc al medicament final. La fase clínica inclou tres etapes:
La fase clínica inclou tres etapes:
Durant el procés d’investigació, moltes molècules amb potencial desapareixen perquè o bé no demostren tenir eficàcia per al que s’està estudiant o bé són tòxiques per a les persones.
ESTUDIS POSTCOMERCIALITZACIÓ: Un cop comercialitzat un nou medicament es realitzen estudis de vigilància i seguretat, ja que el seu ús s'expandeix a milers de persones i en condicions no estudiades en fases anteriors. Aquest estudis s’anomenen de fase IV o estudis de farmacovigilància. Hi participen pacients de tot el món i es fa un seguiment de l'ús del medicament amb l’objectiu principal de detectar efectes adversos addicionals.
Des que s’inicia la fase preclínica fins que finalitzen els estudis postcomercialització poden arribar a passar més de 30 anys. La despesa total del procés s’acosta als 110 milions d’euros.
I recordi: Davant qualsevol dubte consulti al seu metge o farmacèutic.
BIBLIOGRAFIA:
DEPARTAMENT DE SALUT. GENERALITAT DE CATALUNYA. Com es fan els medicaments [En línia]. Barcelona. <http://medicaments.gencat.cat/ca/ciutadania/informacio-i-consells/preguntes-frequents/com-es-fan-els-medicaments/> [Consulta: 2 gener de 2020]
AGENCIA ESPAÑOLA DE MEDICAMENTOS Y PRODUCTOS SANITARIOS. Cómo se regulan los Medicamentos y Productos Sanitarios en España. [En línia]. Madrid.
https://www.aemps.gob.es/publicaciones/publica/regulacion_med-PS/docs/folleto-regulacion_Med-PS.pdf> [Consulta: 2 gener de 2020]